Imunohistokemija Huh7 stanica liječenih BNT162b2 na distribuciji proteina LINE-1
Ovdje smo ispitali učinak BNT162b2 na ekspresiju gena LINE-1. RT-qPCR je proveden na RNK pročišćenom iz Huh7 stanica liječenih BNT162b2 (0, 0,5, 1,0 i 2,0 μg/mL) tijekom 6, 24 i 48 h, koristeći temeljne premaze koji ciljaju LINIJU-1. Značajno povećana ekspresija LINE-1 u usporedbi s kontrolom opažena je pri 6 h za 2,0 μg/mL BNT162b2, dok su niže koncentracije BNT162b2 smanjile izričaj LINE-1 u svim vremenskim točkama.
Razine LINE-1 mRNA u Huh7 stanicama tretiranim BNT162b2. Huh7 stanice tretirane su bez (Ctrl) ili s 0,5 (V1), 1 (V2) i 2 μg/mL (V3) BNT162b2 za 6 (zelene točkice), 24 (crvene točkice) i 48 h (plave točkice). RNK je pročišćena, a qPCR je izveden pomoću prajmera koji ciljaju LINE-1. Razine RNK linije LINE-1 prikazane su kao 2−ΔΔCT vrijednosti u odnosu na gene za čuvanje kuća GAPDH i ACTB. Rezultati su iz pet neovisnih eksperimenata (n = 5). Razlike između odgovarajućih skupina analizirane su pomoću studentovog t-testa s dva kraka. Podaci se izražavaju kao srednja vrijednost ± SEM. (* p < 0,05; ** p < 0,01; *** p < 0,001 u odnosu na odgovarajuću kontrolu u svakoj vremenskoj točki ili kako je naznačeno; † p < 0,05 naspram 6 h-Ctrl).
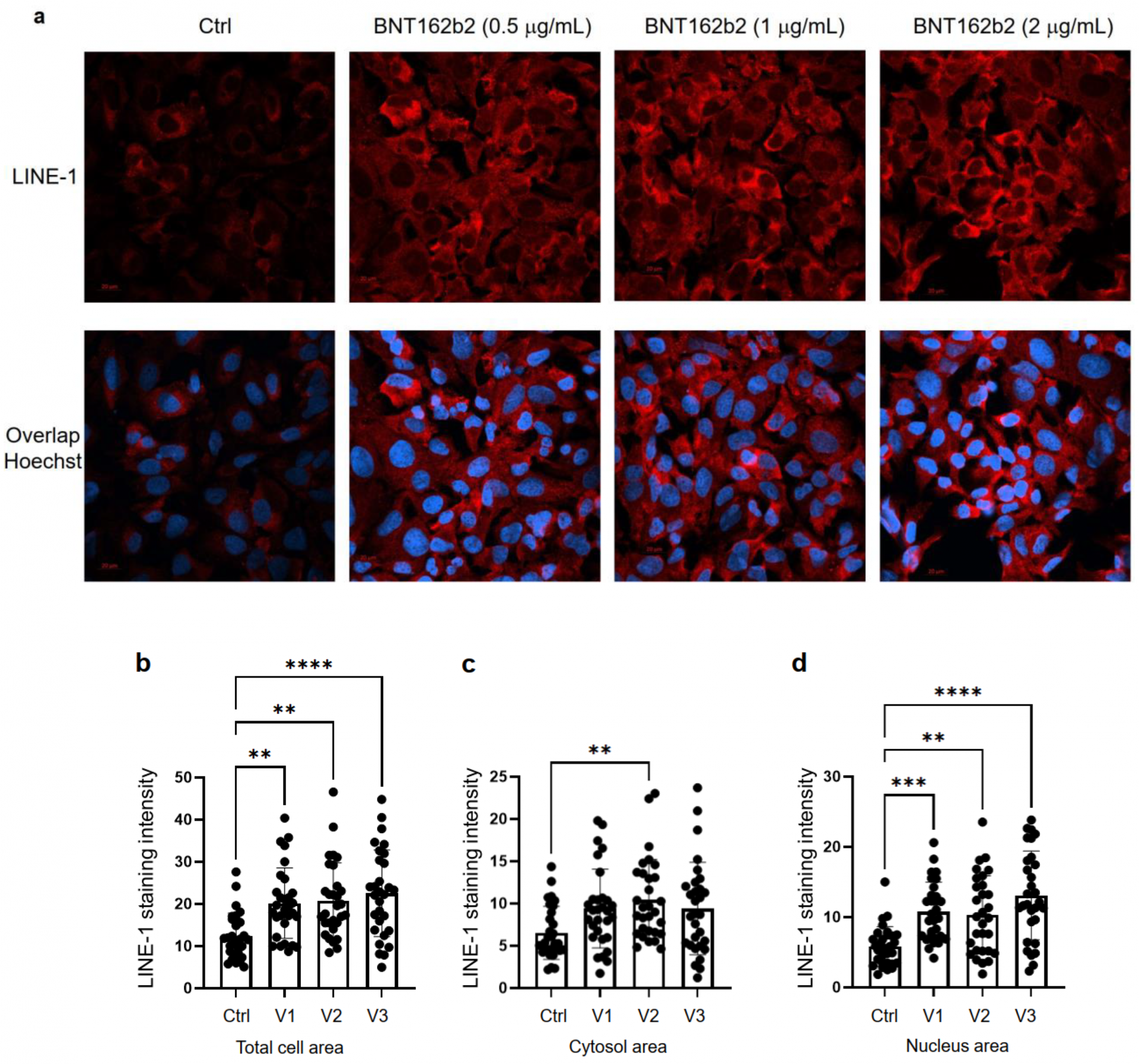
Zatim smo proučavali učinak BNT162b2 na razinu proteina LINE-1. Line-1 u punoj dužini sastoji se od 5′ neprevedene regije (UTR), dva otvorena okvira za čitanje (ORF- ovi), ORF1 i ORF2 i 3′UTR, od kojih je ORF1 RNA vezni protein s pratećom aktivnošću. Dokazano je da aktivnost retrotranspozicije line-1 uključuje translokaciju ORF1 u jezgru[35]. Huh7 stanice liječene ili bez BNT162b2 (0,5, 1,0 i 2,0 μg/mL) tijekom 6 h bile su fiksirane i obojene antitijelima koja se vežu za LINE-1 ORF1p i sondom Hoechst specifičnom za DNK za vizualizaciju stanične jezgre. Kvantifikacija intenziteta bojenja imunofluorescencije pokazala je da je BNT162b2 povećao razinu proteina LINE-1 ORF1p u cijelom staničnom području i jezgri u svim ispitivanim koncentracijama.
Imunohistokemija Huh7 stanica liječenih BNT162b2 na distribuciji proteina LINE-1. Huh7 stanice tretirane su bez (Ctrl) ili s 0,5, 1 i 2 μg/mL BNT162b2 tijekom 6 h. Stanice su fiksirane i obojene antitijelima koja se vežu za LINE-1 ORF1p (crvena) i DNK specifičnu sondu Hoechst za vizualizaciju stanične jezgre (plava). (a) Reprezentativne slike izraza LINE-1 u stanicama Huh7 tretiranim sa ili bez BNT162b2. (b–d) kvantifikacija proteina LINE-1 u cijelom staničnom području (b), citosolu (c) i jezgri (d). Svi podaci analizirani su pomoću jednosmjerne ANOVA-e, a grafikoni su stvoreni pomoću GraphPad Prism V 9.2. Svi podaci prikazani su kao srednji ± SD (** p < 0,01; *** p < 0,001; **** p < 0,0001 kako je naznačeno).
Otkrivanje obrnute transkribirane DNK BNT162b2 u huh7 stanicama
Prethodna studija pokazala je da je ulazak proteina LINE-1 u jezgru povezan s retrotranspozicijom [35]. U gore opisanom eksperimentu bojenja imunofluorescencije, povećane razine LINE-1 u jezgri opažene su već u najnižoj koncentraciji BNT162b2 (0,5 μg/mL). Da bismo ispitali je li BNT162b2 obrnuto transkribiran u DNK kada je LINE-1 povišen, pročistili smo genomsku DNK iz Huh7 stanica tretiranih s 0,5 μg/mL BNT162b2 tijekom 6, 24 i 48 h. Pročišćeni DNK tretiran je RNaseom kako bi se uklonila RNA i podvrgnut PCR-u pomoću prajmera koji ciljaju BNT162b2. Pojačani fragmenti DNK potom su vizualizirani elektroforezom i pročišćenim gelom (slika 5.). Amplikani DNK BNT162b2 otkriveni su u sve tri vremenske točke (6, 24 i 48 h). Sangerovo sekvenciranje potvrdilo je da su DNK ampliksoni identični sekvenci BNT162b2 uz prajmere. Kako bismo osigurali da su DNK amplikoni izvedeni iz DNA, ali ne i BNT162b2 RNK, također smo izveli PCR na RNK pročišćenom iz Huh7 stanica tretiranih s 0,5 μg /mL BNT162b2 tijekom 6 h, sa ili bez RNase tretmana, a u RNK uzorcima RNK podvrgnutim PCR-u nije otkriveno pojačalo.
Figure 5. Detection of DNA amplicons of BNT162b2 in Huh7 cells treated with BNT162b2. Huh7 cells were treated without (Ctrl) or with 0.5 µg/mL of BNT162b2 for 6, 24, and 48 h. Genomic DNK was purified and digested with 100 µg/mL RNase. PCR was run on all samples with primers targeting BNT162b2, as shown in Figure 1 and Table 1. DNA amplicons (444 bps) were visualized on agarose gel. BNT: BNT162b2; L: DNA ladder; Ctrl1: cultured Huh7 cells; Ctrl2: Huh7 cells without BNT162b2 treatment collected at 6 h; Ctrl3: Huh7 cells without BNT162b2 treatment collected at 24 h; Ctrl4: Huh7 cells without BNT162b2 treatment collected at 48 h; Ctrl5: RNA from Huh7 cells treated with 0.5 µg/mL of BNT162b2 for 6 h; Ctrl6: RNA from Huh7 cells treated with 0.5 µg/mL of BNT162b2 for 6 h, digested with RNase.
Rasprava
U ovoj studiji predstavljamo dokaze da cjepivo protiv COVID-19 mRNK BNT162b2 može ući u liniju ljudskih stanica jetre Huh7 in vitro. BNT162b2 mRNK je obrnuto prepisan intracelularno u DNA brzinom od 6 h nakon izlaganja BNT162b2. Mogući mehanizam za reverznu transkripciju je kroz endogenu reverznu transkripciju LINE-1, a distribucija proteina jezgre LINE-1 povišena je za BNT162b2.
Intracelularno nakupljanje LNP-a u hepatocitima dokazano je in vivo [36]. Pretklinička studija na BNT162b2 pokazala je da BNT162b2 ulazi u liniju ljudskih stanica HEK293T stanica i dovodi do robusne ekspresije antigena BNT162b2 [37]. Stoga smo u ovoj studiji prvo istraživali ulazak BNT162b2 u stanice ljudskih stanica jetre Huh7. Izbor koncentracija BNT162b2 korištenih u ovoj studiji zahtijeva objašnjenje. BNT162b2 se primjenjuje kao serija od dvije doze u razmaku od tri tjedna, a svaka doza sadrži 30 μg BNT162b2 u volumenu od 0,3 ml, što lokalnu koncentraciju na mjestu ubrizgavanja čini najvišom 100 μg/mL [31]. Prethodna studija o mRNK cjepivima protiv virusa gripe H10N8 i H7N9 pomoću sličnog sustava isporuke LNP-a pokazala je da se mRNA cjepivo može nespecifično distribuirati na nekoliko organa kao što su jetra, slezena, srce, bubreg, pluća i mozak, a koncentracija u jetri otprilike je 100 puta niža od koncentracije intra-mišićne injekcije [38 ]. U izvješću o procjeni BNT162b2 koje je Pfizer dostavio EMA-i, studije farmakokinetičke distribucije u štakora pokazale su da se relativno velik udio (do 18 %) ukupne doze distribuira u jetru [26]. Stoga smo odlučili koristiti 0,5, 1 i 2 μg/mL cjepiva u našim eksperimentima na stanicama jetre. Međutim, učinak šireg raspona nižih i viših koncentracija BNT162b2 također bi trebalo provjeriti u budućim ispitivanjima.
U trenutnoj studiji, koristili smo liniju ljudskih stanica jetre za in vitro istraživanje. Vrijedi istražiti predstavljaju li stanice jetre također protein šiljaka SARS-CoV-2 dobiven cjepivom, koji bi potencijalno mogao učiniti stanice jetre ciljevima za prethodno premazane proteinske reaktivne citotoksične T stanice proteina šiljka. Bilo je izvješća o pojedincima koji su razvili autoimuni hepatitis [39] nakon cijepljenja BNT162b2. Da bi se postiglo bolje razumijevanje potencijalnih učinaka BNT162b2 na funkciju jetre, in vivo modeli su poželjni za buduće studije.
U izvješću o toksičnosti BNT162b2 nisu provedena ispitivanja genotoksičnosti niti karcinogenosti [26]. Naša studija pokazuje da se BNT162b2 može preokrenuti u DNK u liniji stanica jetre Huh7, a to može dovesti do zabrinutosti ako se DNK dobivena od BNT162b2 može integrirati u genom domaćina i utjecati na integritet genomske DNA, što potencijalno može posredovati genotoksične nuspojave. U ovoj fazi ne znamo je li DNK obrnuto transkribirana iz BNT162b2 integrirana u stanični genom. Potrebna su daljnja istraživanja kako bi se pokazao učinak BNT162b2 na genomski integritet, uključujući sekvenciranje cijelog genoma stanica izloženih BNT162b2, kao i tkiva ljudskih subjekata koji su primili cijepljenje protiv BNT162b2.
Ljudski autonomni retrotranspozon LINE-1 je stanični endogeni reverzni transkriptaza i jedini preostali aktivni transposon kod ljudi, koji može retrotroponirati sebe i druge neautonomne elemente [40,41], a ~17% ljudskog genoma sastoji se od sekvenci LINE-1 [42]. Neautonomni Alu elementi, kratki, mjestimični nukleotidni elementi (SINEs), varijabilni broj-tandem-ponavljanja (VNTR), kao i stanični pseudogeni obrađeni mRNA- om, retrotransponirani su proteinima retrotranspozicije LINE-1 koji djeluju u trans [43,44]. Nedavna studija pokazala je da endogeni LINE-1 posreduje u obrnutom transkripciji i integraciji SARS-CoV-2 sekvenci u genome zaraženih ljudskih stanica [25]. Nadalje, ekspresija endogene LINIJE-1 često se povećava nakon virusne infekcije, uključujući infekciju SARS-CoV-2 [45,46,47]. Prethodna istraživanja pokazala su da je aktivnost retrotranspozicije LINE-1 regulirana metabolizmom RNK [48,49], odgovorom na oštećenje DNA [50], i autofagijom [51]. Učinkovita retrotranspozicija LINE-1 često je povezana s staničnim ciklusom i razgradnjom nuklearne ovojnice tijekom mitoze [52,53], kao i egzogenim retrovirusima [54,55], što potiče ulazak LINE-1 u jezgru. U našoj studiji uočili smo povećanu distribuciju LINE-1 ORF1p kako je određena imunohistokemijom u jezgri BNT162b2 u svim ispitivanim koncentracijama (0,5, 1 i 2 μg/mL), dok je povišena ekspresija gena LINE-1 otkrivena u najvišoj koncentraciji BNT162b2 (2 μg/mL). Važno je napomenuti da je transkripcija gena regulirana modifikacijama kromatina, regulacijom transkripcijskog faktora i stopom razgradnje RNK, dok translacijska regulacija proteina uključuje regrutaciju ribosoma na inicijacijskom kodonu, modulaciju izduženja peptida, prestanak sinteze proteina ili biogenezu ribosoma. Ta dva procesa kontroliraju različiti mehanizmi i stoga možda neće uvijek pokazivati iste obrasce promjena kao odgovor na vanjske izazove. Točna regulacija aktivnosti LINE-1 kao odgovor na BNT162b2 zaslužuje daljnje proučavanje.
Model stanica koji smo koristili u ovoj studiji je linija stanica karcinoma, s aktivnom replikacijom DNK koja se razlikuje od somatskih stanica koje se ne dijele. Također je pokazano da Huh7 stanice pokazuju značajnu različitu ekspresiju gena i proteina, uključujući upregulirane proteine uključene u metabolizam RNK [56]. Međutim, proliferacija stanica također je aktivna u nekoliko ljudskih tkiva kao što su koštana srž ili bazalni slojevi epitela, kao i tijekom embrogeneze, te je stoga potrebno ispitati učinak BNT162b2 na genomski integritet u takvim uvjetima. Nadalje, učinkovita retrotranspozicija LINE-1 također je prijavljena u stanicama koje nisu podijeljene i terminalno diferencirane, kao što su ljudski neuroni [57,58].
Izvješće o procjeni Pfizer EMA-e također je pokazalo da se BNT162b2 distribuira u slezeni (<1,1%), nadbubrežnim žlijezdama (<0,1%), kao i niskoj i mjerljivoj radioaktivnosti u jajnicima i testisima (<0,1%) [26]. Nadalje, podaci o prijenosu posteljice BNT162b2 nisu dostupni iz izvješća o procjeni Pfizer EMA-e. Naši rezultati pokazali su da BNT162b2 mRNK spremno ulazi u Huh7 stanice u koncentraciji (0,5 μg/mL) koja odgovara 0,5% lokalne koncentracije mjesta injiciranja, izaziva promjene u ekspresiji gena i proteina LINE-1, a unutar 6 h može se otkriti reverzna transkripcija BNT162b2. Stoga je važno dodatno istražiti učinak BNT162b2 na druge tipove stanica i tkiva in vitro i in vivo.
Zaključci
Naša studija je prva in vitro studija o utjecaju cjepiva protiv COVID-19 mRNK BNT162b2 na staničnu liniju ljudske jetre. Predstavljamo dokaze o brzom ulasku BNT162b2 u stanice i naknadnom unutarstaničnom obrnutom prijepisu BNT162b2 mRNK u DNK.
Dodatni materijali
Sljedeće popratne informacije možete preuzeti na: https://www.mdpi.com/article/10.3390/cimb44030073/s1.
Autorski doprinosi
M.A., F.O.F., D.Y., M.B. i C.L. izveli su in vitro eksperimente. M.A. i F.O.F. su napravili analizu podataka. M.R. i Y.D.M pridonijeli su provedbi istraživanja, osmislili i nadzirali studiju. Y.D.M. napisao je rad uz doprinos svih autora. Svi autori su pročitali i pristali na objavljenu verziju rukopisa.
Financiranje
Ovu studiju podržalo je Švedsko istraživačko vijeće, Strateško istraživačko područje Exodiab, Dnr 2009-1039, Švedski vladin fond za klinička istraživanja (ALF) i osnivanje Sveučilišne bolnice Skåne.
Priznanja
Autori zahvaljuju Svenu Haidlu, Mariji Josephson, Enmingu Zhangu, Jia-Yi Liju, Caroline Haikal i Pradeepu Bompadi na podršci ovoj studiji.
Sukobi interesa
Autori ne izjavljuju sukob interesa.
Reference:
- Svjetska zdravstvena organizacija. Nadzorna ploča s koronavirusom (COVID-19). Dostupno na internetu: https://covid19.who.int/(pristupljeno 22. veljače 2022.).
- Mulligan, M.J.; Lyke, K.E.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Neuzil, K.; Raabe, V.; Bailey, R.; Swanson, K.A.; i sur. Ispitivanje faze I/II cjepiva protiv COVID-19 RNK BNT162b1 u odraslih. Priroda2020,586, 589–593. [Google scholar] [CrossRef] [PubMed]
- Walsh, E.E.; Frenck, R.W., Mlađi; Falsey, A.R.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Neuzil, K.; Mulligan, M.J.; Bailey, R.; i sur. Sigurnost i imunogenost dvaju kandidata za cjepivo protiv COVID-19 koji se temelje na RNK. Engl. J. Med.2020., 383., 2439.–2450. [Google scholar] [CrossRef] [PubMed]
- Polack, F.P.; Thomas, S.J.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Perez, J.L.; Perez Marc, G.; Moreira, E.D.; Zerbini, C.; i sur. Sigurnost i djelotvornost cjepiva BNT162b2 mRNA COVID-19. Engl. J. Med.2020., 383., 2603.–2615. [Google scholar] [CrossRef] [PubMed]
- Harris, R.J.; Hall, J.A.; Zaidi, A.; Andrews, N.J.; Dunbar, J.K.; Dabrera, G. Učinak cijepljenja na prijenos SARS-CoV-2 u kućanstvu u Engleskoj. Engl. J. Med.2021., 385., 759.–760. [Google scholar] [CrossRef]
- Butt, A.A.; Omer, S.B.; Yan, P.; Shaikh, O.S.; Mayr, F.B. Sars-CoV-2 učinkovitost cjepiva u visokorizičnoj nacionalnoj populaciji u stvarnom okruženju. Pripravnica. Med.2021., 174., 1404.–1408. [Google scholar] [CrossRef]
- Dagan, N.; Barda, N.; Kepten, E.; Miron, O.; Perchik, S.; Katz, M.A.; Hernan, M.A.; Lipsitch, M.; Reis, B.; Balicer, R.D. BNT162b2 mRNA Cjepivo protiv Covida-19 u okruženju masovnog cijepljenja diljem zemlje. Engl. J. Med.2021., 384., 1412.–1423. [Google scholar] [CrossRef]
- Rossman, H.; Shilo, S.; Meir, T.; Gorfine, M.; Shalit, U.; Segal, E. COVID-19 dinamika nakon nacionalnog programa imunizacije u Izraelu. Med.2021., 27., 1055.–1061. [Google scholar] [CrossRef]
- Ventilator, B.E.; Shen, J.Y.; Lim, X.R.; Tu, T.M.; Chang, C.C.R.; Khin, H.S.W.; Koh, J.S.; Rao, J.P.; Lau, S.L.; Tan, G.B.; i sur. Cerebralna venska tromboza nakon cijepljenja protiv BNT162b2 mRNA SARS-CoV-2: Događaj crnog labuda. Ja sam J. Hematol., 96., E357–E361. [Google scholar] [CrossRef]
- Larson, K.F.; Ammirati, E.; Adler, E.D.; Cooper, L.T., mlađi; Hong, K.N.; Saponara, G.; Couri, D.; Cereda, A.; Procopio, A.; Cavalotti, C.; i sur. Miokarditis Nakon cijepljenja BNT162b2 i mRNA-1273. Cirkulacija2021, 144, 506–508. [Google scholar] [CrossRef]
- Menni, C.; Klasar, K.; Svibanj, A.; Polidori, L.; Capdevila, J.; Louca, P.; Sudre, C.H.; Nguyen, L.H.; Drew, D.A.; Merino, J.; i sur. Nuspojave cjepiva i infekcija SARS-CoV-2 nakon cijepljenja kod korisnika aplikacije COVID Symptoms Study u Velikoj Britaniji: Buduća opservacijska studija. Lancet Infect. Dis.2021., 21., 939.–949. [Google scholar] [CrossRef]
- Hansen, T.; Titze, U.; Kulamadayil-Heidenreich, N.S.A.; Glombitza, S.; Tebbe, J.J.; Rocken, C.; Schulz, B.; Weise, M.; Wilkens, L. Prvi slučaj obdukcijskog ispitivanja u bolesnika cijepljenog protiv SARS-CoV-2. J. Infect. Dis.2021., 107., 172.–175. [Google scholar] [CrossRef] [PubMed]
- Kadali, R.A.K.; Janagama, R.; Peruru, S.; Malayala, S.V. Nuspojave cjepiva BNT162b2 mRNA COVID-19: Randomizirana, presječna studija s detaljnim samoprocjenom simptoma zdravstvenih radnika. J. Infect. Dis.2021., 106., 376.–381. [Google scholar] [CrossRef] [PubMed]
- Parkash, O.; Sharko, A.; Farooqi, A.; Ying, G.W.; Sura, P. Akutni pankreatitis: Moguća nuspojava cjepiva protiv COVID-19. Cureus2021, 13, e14741. [Google scholar] [CrossRef] [PubMed]
- Mazzatenta, C.; Piccolo, V.; Tempo, G.; Romano, ja.; Argenziano, G.; Bassi, A. Purpuric lezije na kapcima razvijene nakon cjepiva BNT162b2 mRNA COVID-19: Još jedan komad SARS-CoV-2 kožne slagalice? Acad. Dermatol. Venereol.2021., 35., e543– e545. [Google scholar] [CrossRef]
- Lee, E.J.; Cines, D.B.; Gernsheimer, T.; Kessler, C.; Michel, M.; Tarantino, dr.med.; Semple, J.W.; Arnold, D.M.; Godeau, B.; Lambert, M.P.; i sur. Trombocitopenija nakon cijepljenja Pfizer i Moderna SARS-CoV-2. Ja sam J. Hematol.2021., 96., 534.–537. [Google scholar] [CrossRef]
- Ishay, Y.; Kenig, A.; Tsemach-Toren, T.; Amer, R.; Rubin, L.; Hershkovitz, Y.; Kharouf, F. Autoimuni fenomeni nakon cijepljenja protiv SARS-CoV-2. 2021., 99., 107970. [Google scholar] [CrossRef]
- Das, B.B.; Kohli, Sjedinjene Američke Države; Ramachandran, P.; Nguyen, H.H.; Greil, G.; Hussain, T.; Tandon, A.; Kane, C.; Avula, S.; Duru, C.; i sur. Mioperikarditis nakon mRNA COVID-19 Cijepljenje u adolescenata u dobi od 12 do 18 godina. Pediatr.2021., 238., 26.–32.e1. [Google scholar] [CrossRef]
- McLaurin-Jiang, S.; Garner, C.D.; Krutsch, K.; Hale, T.W. Simptomi majke i djeteta nakon cijepljenja protiv COVID-19 među majkama koje doje. Med.2021., 16., 702.–709. [Google scholar] [CrossRef]
- Barda, N.; Dagan, N.; Ben-Shlomo, Y.; Kepten, E.; Waxman, J.; Ohana, R.; Hernan, M.A.; Lipsitch, M.; Kohane, I.; Netzer, D.; i sur. Sigurnost cjepiva BNT162b2 mRNA Covid-19 u nacionalnom okruženju. Engl. J. Med.2021., 385., 1078.–1090. [Google scholar] [CrossRef]
- Baden, L.R.; El Sahly, H.M.; Essink, B.; Kotloff, K.; Frey, S.; Novak, R.; Diemert, D.; Spector, S.A.; Rouphael, N.; Creech, C.B.; i sur. Djelotvornost i sigurnost cjepiva protiv mRNA-1273 SARS-CoV-2. Engl. J. Med.2021., 384., 403.–416. [Google scholar] [CrossRef]
- Sadoff, J.; Siva, G.; Vandebosch, A.; Cardenas, V.; Shukarev, G.; Grinsztejn, B.; Goepfert, P.A.; Truyers, C.; Fennema, H.; Špijuni, B.; i sur. Sigurnost i djelotvornost jednodoznog cjepiva Ad26.COV2.S protiv Covida-19. Engl. J. Med.2021., 384., 2187.–2201. [Google scholar] [CrossRef] [PubMed]
- Eichinger, S.; Warkentin, T.E.; Greinacher, A. Trombotička trombocitopenija nakon cijepljenja ChAdOx1 nCoV-19. Odgovor. Engl. J. Med.2021., 385., e11. [Google scholar] [CrossRef] [PubMed]
- Doroftei, B.; Ciobica, A.; Ilie, O.D.; Maftei, R.; Ilea, C. Mini-pregled koji raspravlja o pouzdanosti i učinkovitosti cjepiva protiv COVID-19. Dijagnostika2021, 11, 579. [Google scholar] [CrossRef]
- Zhang, L.; Richards, A.; Barrasa, M.I.; Hughes, S.H.; Mladi, R.A.; Jaenisch, R. Obrnuto-transkribirani SARS-CoV-2 RNA može se integrirati u genom kultiviranih ljudskih stanica i može se izraziti u tkivima dobivenim od pacijenta. Natl. Acad. Sci. USA2021, 118, e2105968118. [Google scholar] [CrossRef] [PubMed]
- Dostupno na internetu: https://www.ema.europa.eu/en/documents/assessment-report/comirnaty-epar-public-assessment-report_en.pdf(pristupljeno 24. veljače 2022.).
- Tanaka, H.; Takata, N.; Sakurai, Y.; Yoshida, T.; Inoue, T.; Tamagawa, S.; Nakai, Y.; Tange, K.; Yoshioka, H.; Maeki, M.; i sur. Isporuka Oligonukleotida pomoću samorazgradivog lipidnog materijala. Farmaceutika2021, 13, 544. [Google scholar] [CrossRef]
- Sedić, M.; Senn, J.J.; Lynn, A.; Laska, M.; Smith, M.; Platz, S.J.; Bolen, J.; Hoge, S.; Bulychev, A.; Jacquinet, E.; i sur. Procjena sigurnosti lipidne nanočestica formulirane modificirane mRNA u Sprague-Dawley Rat i Cynomolgus Monkey. Veterinar Pathol., 55., 341.–354. [Google scholar] [CrossRef]
- Sato, Y.; Matsui, H.; Yamamoto, N.; Sato, R.; Munakata, T.; Kohara, M.; Harashima, H. Vrlo specifična isporuka siRNA-e hepatocitima zaobilazi endotelnu staničnu toksičnost povezanu s lipidnim nanočesticama koja dovodi do sigurnog i učinkovitog smanjenja virusa hepatitisa B. Kontrola. Izdanje2017, 266, 216–225. [Google scholar] [CrossRef]
- Heidel, J.D.; Yu, Z.; Liu, J.Y.; Rele, S.M.; Liang, Y.; Zeidan, R.K.; Kornbrust, D.J.; Davis, M.E. Administracija u neljudskim primatima eskalacije intravenskih doza ciljanih nanočestica koje sadrže ribonukleotid reduktazu podjedinica M2 siRNA. Natl. Acad. Sci. USA2007, 104, 5715–5721. [Google scholar] [CrossRef]
- Dostupno na internetu: https://www.cvdvaccine-us.com/(pristupljeno 24. veljače 2022.).
- Dostupno na internetu: http://bridgeslab.sph.umich.edu/protocols/index.php/Preparation_of_Tail_Samples_(for_Genotyping)(pristupljeno 24. veljače 2022.).
- Gallud, A.; Munson, M.J.; Liu, K.; Idstrom, A.; Barriga, H.M.; Tabaei, S.; Aliakbarinodehi, N.; Ojansivu, dr.; Lubart, Q.; Doutch, J.J.; i sur. Vremenska evolucija prolijevanja PEG-a i krunidbe proteina u serumu određuje kinetiku unosa stanica i isporuku lipidnih nanočestica. bioRxiv2021. [Google scholar] [CrossRef]
- Svjetska zdravstvena organizacija Messenger RNA kodiranje cjelovečernje SARS-CoV-2 Spike glikoprotein. 2020. Dostupno na internetu: https://web.archive.org/web/20210105162941/https://mednet-communities.net/inn/db/media/docs/11889.doc(pristupljeno 24. veljače 2022.).
- Mita, P.; Wudzinska, A.; Sunce, X.; Andrade, J.; Nayak, S.; Kahler, D.J.; Badri, S.; LaCava, J.; Ueberheide, B.; Yun, C.Y.; i sur. LOKALIZACIJA proteina LINE-1 i funkcionalna dinamika tijekom staničnog ciklusa. Elife2018, 7, e30058. [Google scholar] [CrossRef]
- Sato, Y.; Kinami, Y.; Hashiba, K.; Harashima, H. Različite kinetike za unos jetre lipidnih nanočestica između apolipoproteina E/ lipoprotein receptora niske gustoće i N-acetil-d-galaktozamin / asialoglycoprotein receptora put. Kontrola. Izdanje2020, 322, 217–226. [Google scholar] [CrossRef]
- Vogel, A.B.; Kanevsky, I.; Che, Y.; Swanson, K.A.; Muik, A.; Vormehr, M.; Kranz, L.M.; Walzer, K.C.; Hein, S.; Guler, A.; i sur. Cjepiva BNT162b štite resus makakije od SARS-CoV-2. Priroda2021, 592, 283–289. [Google scholar] [CrossRef] [PubMed]
- Bahl, K.; Senn, J.J.; Yuzhakov, O.; Bulychev, A.; Brito, L.A.; Hassett, K.J.; Laska, M.E.; Smith, M.; Almarsson, O.; Thompson, J.; i sur. Pretklinička i klinička demonstracija imunogenosti mRNA cjepivima protiv virusa gripe H10N8 i H7N9. Ther.2017., 25., 1316.–1327. [Google scholar] [CrossRef] [PubMed]
- Bril, F.; Al Diffalha, S.; Dean, M.; Fettig, D.M. Autoimuni hepatitis koji se razvija nakon cjepiva protiv bolesti koronavirusa 2019(COVID-19): Uzročnost ili žrtva? Hepatol.2021., 75., 222.–224. [Google scholar] [CrossRef]
- Kazazian, H.H., mlađi; Moran, J.V. Mobilni DNK u zdravlju i bolesti. Engl. J. Med.2017., 377., 361.–370. [Google scholar] [CrossRef] [PubMed]
- Coffin, J.M.; Fan, H. Otkriće obrnutog transkriptaze. Velečasni Virol.2016,3, 29–51. [Google scholar] [CrossRef]
- Lander, E.S.; Linton, L.M.; Birren, B.; Nusbaum, C.; Zody, M.C.; Baldwin, J.; Devon, K.; Dewar, K.; Doyle, M.; FitzHugh, W.; i sur. Početno sekvenciranje i analiza ljudskog genoma. Priroda2001, 409, 860–921. [Google scholar] [CrossRef]
- Ostertag, E.M.; Goodier, J.L.; Zhang, Y.; Kazazian, H.H., Jr. SVA elementi su neautonomni retrotranspozoni koji uzrokuju bolesti kod ljudi. Hum. Genet.2003., 73., 1444.–1451. [Google scholar] [CrossRef]
- Hancks, D.C.; Kazazian, H.H., Jr. Aktivni ljudski retrotranspozoni: varijacije i bolesti. Opin. Genet. Dev.2012., 22., 191.–203. [Google scholar] [CrossRef]
- Jones, R.B.; Pjesma, H.; Xu, Y.; Garnizon, K.E.; Buzdin, A.A.; Anwar, N.; Hunter, D.V.; Mujib, S.; Mihajlović, V.; Martin, E.; i sur. LINE-1 retrotransponabilni element DNA se nakuplja u stanicama zaraženim HIV-1. Virol.2013., 87., 13307.–13320. [Google scholar] [CrossRef]
- Macchietto, M.G.; Langlois, R.A.; Shen, S.S. Virus-inducirani transponabilni element izraziti up-regulaciju u ljudskim i mišjim stanicama domaćina. Life Sci. Alliance2020, 3, e201900536. [Google scholar] [CrossRef] [PubMed]
- Yin, Y.; Liu, X.Z.; On, X.; Zhou, L.Q. Egzogeni koronavirus komunicira s endogenim retrotranspozonom u ljudskim stanicama. Infekcija ćelije. Mikrobiol.2021., 11., 609160. [Google scholar] [CrossRef] [PubMed]
- Belancio, V.P.; Roy-Engel, A.M.; Deininger, P. Utjecaj više mjesta spojnice u ljudskim L1 elementima. Gen2008, 411, 38–45. [Google scholar] [CrossRef] [PubMed]
- Dai, L.; Taylor, M.S.; O’Donnell, K.A.; Boeke, J.D. Poly(A) obvezujući protein C1 neophodan je za učinkovitu L1 retrotranspoziciju i utječe na stvaranje L1 RNP-a. Cell Biol.2012., 32., 4323.–4336. [Google scholar] [CrossRef]
- Sluga, G.; Streva, V.A.; Derbes, R.S.; Wijetunge, M.I.; Neeland, M.; Bijela, T.B.; Belancio, V.P.; Roy-Engel, A.M.; Deininger, P.L. Put popravka nukleotida ograničava retrotranspoziciju L1. Genetika2017,205, 139–153. [Google scholar] [CrossRef]
- Guo, H.; Chitiprolu, M.; Gagnon, D.; Meng, L.; Perez-Iratxeta, C.; Lagace, D.; Gibbings, D. Autofagy podržava genomsku stabilnost razgradnjom retrotranspozonske RNK. Komuna.2014,5, 5276. [Google scholar] [CrossRef]
- Xie, Y.; Prijatelji, L.; Ivics, Z.; Izsvak, Z.; Martin, S.L.; A, W. Cell divizija promiče učinkovitu retrotranspoziciju u stabilnoj L1 reporterskoj ćeliji. DNK2013, 4, 10. [Google scholar] [CrossRef]
- Shi, X.; Seluanov, A.; Za retrotranspoziciju L1 potrebna je gorbunova, V. Stanična podjela. Cell Biol.2007., 27., 1264.–1270. [Google scholar] [CrossRef]
- Goff, S.P. Faktori domaćina koje iskorištavaju retrovirusi. Velečasni Mikrobiol2007, 5, 253–263. [Google scholar] [CrossRef]
- Suzuki, Y.; Craigie, R. Put do kromatina – nuklearni ulazak retrovirusa. Velečasni mikrobiol.2007., 5., 187.-196. [Google scholar] [CrossRef]
- Shi, J.; Wang, X.; Lyu, L.; Jiang, H.; Zhu, H.J. Usporedba ekspresije proteina između ljudske jetre i linija jetrenih stanica HepG2, Hep3B i Huh7 pomoću SWATH i MRM-HR proteomike: Fokusiranje na enzime koji metaboliziraju lijekove. Droga Metab. Farmakokinet., 33., 133.–140. [Google scholar] [CrossRef] [PubMed]
- Kubo, S.; Seleme, M.C.; Soifer, H.S.; Perez, J.L.; Moran, J.V.; Kazazian, H.H., mlađi; Kasahara, N. L1 retrotranspozicija u nepodijeljenim i primarnim ljudskim somatskim stanicama. Natl. Acad. Sci. USA2006, 103, 8036–8041. [Google scholar] [CrossRef] [PubMed]
- Macia, A.; Widmann, T.J.; Heras, S.R.; Ayllon, V.; Sanchez, L.; Benkaddour-Boumzaouad, dr.; Munoz-Lopez, M.; Rubio, A.; Amador-Cubero, S.; Blanco-Jimenez, E.; i sur. Projektirana retrotranspozicija LINE-1 u nepodijeljenim ljudskim neuronima. Genom Res.2017., 27., 335.–348. [Google scholar] [CrossRef] [PubMed)